जल (अणु)
जल (H2O) पृथ्वी की सतह पर सर्वाधिक मात्रा में पाया जाने वाला अणु है, जो इस ग्रह की सतह के 70% का गठन करता है। प्रकृति में यह तरल, ठोस और गैसीय अवस्था में मौजूद है। मानक दबावों और तापमान पर यह तरल और गैस अवस्थाओं के बीच गतिशील संतुलन में रहता है। घरेलू तापमान पर, यह तरल रूप में हल्की नीली छटा वाला बेरंग, बेस्वाद और बिना गंध का होता है। कई पदार्थ, जल में घुल जाते हैं और इसे सामान्यतः सार्वभौमिक विलायक के रूप में सन्दर्भित किया जाता है। इस वजह से, प्रकृति में मौजूद जल और प्रयोग में आने वाला जल शायद ही कभी शुद्ध होता है और उसके कुछ गुण, शुद्ध पदार्थ से थोड़ा भिन्न हो सकते हैं। हालांकि, ऐसे कई यौगिक हैं जो कि अनिवार्य रूप से, अगर पूरी तरह नहीं, जल में अघुलनशील है। जल ही ऐसी एकमात्र चीज़ है जो पदार्थ की सामान्य तीन अवस्थाओं में स्वाभाविक रूप से पाया जाता है - अन्य चीज़ों के लिए रासायनिक गुण देखें. पृथ्वी पर जीवन के लिए जल आवश्यक है।[3] जल आम तौर पर, मानव शरीर के 55% से लेकर 78% तक का निर्माण करता है।[4]
जल के रूप
कई पदार्थों की तरह, जल, कई रूप ले सकता है जिसे मोटे तौर पर पदार्थ की प्रावस्था द्वारा वर्गीकृत किया गया है। तरल प्रावस्था जल के रूपों में सबसे आम है और यह वह रूप है जिसे आम तौर पर "जल" शब्द द्वारा अंकित किया जाता है। जल की ठोस प्रावस्था को बर्फ के रूप में जाना जाता है और आम तौर पर यह ठोस, मिश्रित क्रिस्टल जैसी संरचना का रूप लेता है जैसे आइस क्यूब, या नरम रूप से एकीकृत दानेदार क्रिस्टल जैसे हिम का रूप लेता है। ठोस H2O के विभिन्न प्रकार के क्रिस्टलीय और अनाकार स्वरूप की सूची के लिए, बर्फ लेख देखें. जल की गैसीय प्रावस्था को वाष्प (या भाप) जाना जाता है और इसे जल के एक पारदर्शी बादल का विन्यास धारण करने से पहचाना जाता है। जल की चौथी प्रावस्था, सुपर क्रिटिकल तरल, जो अन्य तीन रूपों की तुलना में आम नहीं है प्रकृति में शायद ही कभी घटित होती है। जब जल एक विशेष सूक्ष्म तापमान और एक विशेष सूक्ष्म दबाव (647 K और 22.064 MPa) पर पहुंच जाता है तो तरल और गैस प्रावस्था एक समरूप द्रव प्रावस्था में मिल जाती हैं, जब गैस और तरल, दोनों के गुण मौजूद होते हैं। चूंकि चरम तापमान या दबाव के तहत, जल अत्यंत सूक्ष्म हो जाता है, यह लगभग कभी स्वाभाविक रूप से नहीं होता है। जल के, स्वाभाविक रूप से अत्यंत सूक्ष्म होने का एक उदाहरण गहरे पानी के हाइड्रोथर्मल वेंट के सबसे गर्म हिस्से, जिसमें जल को ज्वालामुखी प्लूम द्वारा सूक्ष्म तापमान तक गर्म किया जाता है और यह सागर की चरम गहराई में कुचल देने वाले वजन की वजह से सूक्ष्म दबाव को प्राप्त करता है, जहां ज्वालामुखी का मुख स्थित है।
प्राकृतिक जल में (देखें मानक मीन महासागर जल), लगभग सभी हाइड्रोजन परमाणु आइसोटोप प्रोटियम होते हैं, 1H. भारी जल वह जल है जिसमें हाइड्रोजन को इसके भारी आइसोटोप, ड्युरेटियम द्वारा प्रतिस्थापित किया जाता है2H. यह रासायनिक रूप से सामान्य जल के समान है लेकिन उसका समरूप नहीं है। इसका कारण यह है कि ड्युरेटियम का नाभिक प्रोटियम की तुलना में दुगुना है और इस तरह ऊर्जा की बॉन्डिंग में और हाइड्रोजन बॉन्डिंग में स्पष्ट मतभेद का कारण बनता है। भारी जल का प्रयोग परमाणु रिएक्टर उद्योग में न्यूट्रॉन को मध्यम (धीमा) करने के लिए किया जाता है। इसके विपरीत, हल्के जल में प्रोटियम आइसोटोप होता है, भेद करने की जरूरत के सन्दर्भों में. एक उदाहरण है लाईट वॉटर रिएक्टर, यह जताने के लिए कि रिएक्टर में हल्के जल का उपयोग होता है।
भौतिकी और रसायन शास्त्र
- इन्हें भी देखें: water chemistry analysis
जल, रासायनिक फार्मूला वाला रासायनिक पदार्थ है: जल के एक अणु में दो हाइड्रोजन परमाणु होते हैं जो ऑक्सीजन के एक परमाणु से बंधे होते हैं।[5]सामान्य परिवेश के तापमान और दबाव में जल एक बेस्वाद, बिना गंध का तरल पदार्थ है और छोटी मात्रा में बेरंग प्रकट होता है, हालांकि आतंरिक रूप से इसमें हल्का नीला रंग देखा जा सकता है। बर्फ भी रंगहीन प्रतीत होता है और वाष्प अनिवार्य रूप से गैस के रूप में अदृश्य होता है।[1] मानक स्थितियों में जल मुख्य रूप से एक तरल होता है, जिसे आवधिक तालिका में ऑक्सीजन परिवार के अन्य समान हाईड्राइड के साथ (हाइड्रोजन सल्फाइड जैसी गैसें) उसके सम्बन्ध के कारण पूर्वानुमान नहीं लगाया जाता. इसके अलावा, आवधिक तालिका में ऑक्सीजन को घेरे हुए तत्त्व, नाइट्रोजन, फ्लोरीन, फास्फोरस, सल्फर और क्लोरीन, सभी, हाइड्रोजन के साथ मानक स्थितियों के तहत गैसों का निर्माण करने के लिए संयुक्त हो जाते हैं। पानी के तरल रूप में होने का कारण यह है कि, इसमें ऑक्सीजन, अन्य सभी तत्वों की तुलना में अधिक इलेक्ट्रोनिगेटिव है, फ्लोरीन के अपवाद के साथ. ऑक्सीजन, हाइड्रोजन की तुलना में इलेक्ट्रॉनों को अधिक जोर से आकर्षित करता है, जिससे हाइड्रोजन परमाणुओं पर एक शुद्ध सकारात्मक चार्ज आता है और ऑक्सीजन परमाणु पर एक शुद्ध नकारात्मक चार्ज. इन प्रत्येक परमाणुओं पर एक चार्ज की उपस्थिति, जल के प्रत्येक अणु को एक शुद्ध डाईपोल क्षण देती है। डाईपोल की वजह से पानी के अणुओं के बीच यह आकर्षण, व्यक्तिगत अणुओं को एक साथ करीब खींचता है, जिससे इन अणुओं को अलग करना और अधिक कठिन हो जाता है और क्वथनांक बिंदु उच्च हो जाता है। इस आकर्षण को हाइड्रोजन बॉन्डिंग के रूप में जाना जाता है। जल के अणु, एक-दूसरे के परिप्रेक्ष्य में लगातार चलायमान रहते हैं और हाइड्रोजन बांड लगातार खंडित और जुड़ते रहते हैं और टाइमस्केल पर यह 200 फेम्टोसेकंड से अधिक तेजी से होता है।[6] हालांकि, यह बॉन्ड, इस लेख में वर्णित पानी के कई विशिष्ट गुणों को बनाने में पर्याप्त मजबूत है, जैसे कि वे गुण जो इसे जीवन का अभिन्न अंग बनाते हैं। जल को एक ध्रुवीय तरल के रूप में वर्णित जा सकता है जो गैर-अनुपातिक रूप से हाइड्रोनियम आयन में थोड़ा असम्बद्ध होता है (H3O+(aq)) और एक संबद्ध हाइड्रॉक्साइड आयन (OH-(aq)).
- 2H2O (l)
 H3O+(aq) + OH-(aq)
H3O+(aq) + OH-(aq)
इस पृथक्करण के लिए निरंतर पृथक्करण को आम तौर पर Kw चिह्न से अंकित करते हैं और इसका मूल्य है 25 °C पर 10−14, अधिक जानकारी के लिए देखें "जल (डेटा पृष्ठ)" और "जल का स्व-आयनाईजेशन.
जल, बर्फ और वाष्प
ताप क्षमता और वाष्पीकरण और फ्यूजन का ताप
सभी ज्ञात पदार्थों में, अमोनिया के बाद पानी में दूसरे स्थान पर उच्चतम विशिष्ट ताप क्षमता होती है, साथ ही उच्च वाष्पीकरण ताप (40.65 kJ• mol−1) होता है, दोनों ही, जल के अणुओं के बीच व्यापक हाइड्रोजन बॉन्डिंग के परिणामस्वरूप होते हैं। ये दो असामान्य गुण, जल को तापमान में अत्यधिक उतार-चढ़ाव के साथ पृथ्वी की जलवायु को मध्यम बनाए रखने की अनुमति देते हैं।
जल की संलयन की तापीय धारिता 0 डिग्री सेल्सियस पर विशिष्ट रूप से 333.55 kJ.kg−1 है। आम पदार्थों में केवल अमोनिया का अधिक है। यह गुण बर्फ बहाव और ग्लेशियर की बर्फ को पिघलने से रोकता है। यांत्रिक प्रशीतन के आगमन से पहले, बर्फ का उपयोग भोजन को सड़ने से रोकने के लिए आम था (और अभी भी है).
जल और बर्फ का घनत्व
जल का घनत्व उसके तापमान पर निर्भर करता है, लेकिन यह संबंध रैखिक नहीं है और मोनोटोनीक भी नहीं है (दाईं-ओर की तालिका देखें). जब जल को कमरे के तापमान से भी अधिक ठंडा किया जाता है, तब वह अन्य पदार्थों की तरह तेजी से घना होने लगता है। लेकिन लगभग 4 °C में, जल अपने अधिकतमघनत्व तक पहुँचता है। जैसे ही उसे परिवेशिक परिस्थितियों में और अधिक ठंडा किया जाता है, तो वह फैल कर कम सघन हो जाती है। यह असामान्य नकारात्मक थर्मल विस्तार, अनुकूलन-आधारित इन्टरमॉलिक्युलर अंतःक्रिया के लिए जिम्मेदार है और पिघले सिलिका मे भी यह देखा गया है।[11]
अधिकांश पदार्थों के ठोस अवस्था उनके तरल अवस्था से अधिक घनी होती है, इसलिए ठोस पदार्थ का एक टुकड़ा तरल पदार्थ में डूब जाता है। लेकिन, इसके विपरीत सामान्य बर्फ का एक टुकड़ा तरल जल में तैरता है, क्योंकि बर्फ का घनत्व तरल जल से कम होता है। ठंडा होने पर, सामान्य बर्फ का घनत्व लगभग 9% कम हो जाता है।[12] इसका कारण है इंटरमॉलिक्युलर तरंगों का ठंडा होना जिससे अणु अपने पड़ोसियों के साथ मजबूत हाइड्रोजन बांड बनाते हैं और षट्कोणीयबर्फ IH के ठंडा होने से हेक्सागोनल पैकिंग हासिल करते हैं। हालांकि हाइड्रोजन बांड, तरल की तुलना में क्रिस्टल में छोटे होते हैं, यह लॉकिंग प्रभाव, तरल के नाभिकीयन के पास पहुंचने के साथ औसत समन्वय संख्या को कम करता है। अन्य पदार्थ, जो ठंडे होने पर विस्तार करते हैं, सुरमा, विस्मुट, गैलियम, जर्मेनियम, सिलिकॉन, एसिटिक एसिड हैं।
केवल साधारण, हेक्सागोनल बर्फ ही तरल से कम घना होता है। बढ़ते दबाव में बर्फ में कई बदलाव होते हैं, जो तरल पानी से उच्च घनत्व वाले होते हैं, जैसे अनाकार बर्फ (HDA) और बहुत ही उच्च घनत्व वाले अनाकार बर्फ (VHDA).
तापमान मे बढ़त के साथ जल का फैलाव भी बढ़ता है। उच्चतम बिन्दु तक पहुंचते हुए जल का घनत्व अपने उच्चतम मान से 4% कम हो जाता है।
एक मानक दबाव मे बर्फ के पिघलने की सीमा बिंदु 0 डिग्री सेल्सियस (32 °F, 273 K) होती है, हालांकि, शुद्ध तरल जल को बिना जमाये उस तापमान से नीचे के तापमान मे भी बेहतरीन तरीके से शीतल किया जा सकता है, यदी तरल पदार्थ को हिलाया न जाए. यह अपने समरूप नाभिकीयन बिन्दु जो लगभग 231 के (-42°सी)[13] तक एक द्रव स्वरूप में ही रह सकता है। साधारण षट्कोणीय बर्फ का गलनांक, उच्च दबाव se थोड़ा नीचे गिरता है, लेकिन जब बर्फ अपने एलोट्रोप्स में बदलता है (बर्फ का क्रिस्टलीय रूप देखें), तो गलनांक, दबाव के साथ काफी बढ़ जाता है, जो 355 के (82 °से.) पर 2.216 Gपास्कल (21,870 परमाणु)(बर्फ VII के त्रिगुण बिन्दु).[14]
साधारण बर्फ के गलनांक को कम करने के लिए एक महत्वपूर्ण दबाव की आवश्यकता होती है - एक आइस स्केटर द्वारा डाला गया दबाव, गलनांक बिंदु को केवल लगभग 0.09 °C (0.16 °F) कम करता है।[कृपया उद्धरण जोड़ें]
जल के इन गुणों की पृथ्वी के पारिस्थितिकी तंत्र में महत्वपूर्ण भूमिका होती है। 4 डिग्री सेल्सियस के तापमान का जल, वातावरण में किसी भी तापमान के बावजूद, हमेशा ताजे जल की झीलों के तल में जमा हो जाता है। चूंकि जल और बर्फ, ऊष्मा के खराब चालक है[15], (विसंवाहक) ऐसी संभावना नहीं रहती है कि पर्याप्त गहरी झील पूरी तरह से जम जायेगी, जब तक कि उसे शक्तिशाली धाराओं द्वारा हिलाया न जाए जिससे ठंडा और गर्म पानी मिल जाएगा और शीतलीकरण को तेज़ करेगा। गर्म मौसम में, बर्फ की चट्टानें, नीचे डूबने की बजाय, जहां वे बहुत धीरे-धीरे पिघलती हैं, तैरती हैं। ये घटनाएं इस प्रकार जलीय जीवन की रक्षा कर सकती हैं।
खारेजल और बर्फ का घनत्व
जल का घनत्व, जल में घुले नमक और साथ ही जल के तापमान पर निर्भर करता है। बर्फ अभी भी महासागरों में तैरते हैं, अन्यथा वे नीचे से ऊपर की ओर जम जायेंगे. हालांकि, महासागरों में नमक की मात्रा हिमांक को 2 डिग्री सेल्सियस कम कर देती है और जल के अधिकतम घनत्व के तापमान को हिमांक तक कम कर देता है। यही कारण है कि, समुद्री जल में, पानी का नीचे की ओर संवहन, पानी के फैलने से बाधित नहीं होता है चूंकि यह हिमांक के नज़दीक ठंडा हो जाता है। महासागरों का ठंडा जल, हिमांक के निकट नीचे जाता रहता है। इस कारण से, कोई भी प्राणी जो आर्कटिक महासागर जैसे ठन्डे पानी के तल में जीवित रहने का प्रयास करता है, सामान्यतः सर्दियों में किसी झील के जमे हुए ठंडे पानी से 4 °C से भी कम के तापमान पर रहेगा.[तथ्य वांछित]
जैसे-जैसे सतह का खारा जल जमना शुरू होता है (-1.9 सामान्य लवणता वाले समुद्री जल के लिए), जो बर्फ बनता है वह अनिवार्य रूप से लवण मुक्त होता है और उसका घनत्व मीठे जल के बराबर होता है। बर्फ के बहते खंड और जमा हुआ नमक भी समुद्री जल की लवणता और घनत्व को प्रभावित करता है, इस प्रक्रिया को ब्राइन रिजेक्शन के रूप में जाना जाता है। यह अधिक घनत्व वाला खारा जल, संवहन द्वारा नीचे जाता है और उसकी जगह पर आने वाला समुद्री जल उसी समान प्रक्रिया से गुज़रता है। इससे सतह पर -1.9 डिग्री सेल्सियस पर अनिवार्य रूप से मीठे जल का बर्फ प्राप्त होता है। जमी बर्फ के नीचे समुद्री जल के घनत्व में वृद्धि उसे नीचे की ओर डुबाने का कारण बनता है। एक बड़े पैमाने पर, ब्राइन रिजेक्शन की प्रक्रिया और समुद्र के ठंडे नमकीन जल को डुबाने के परिणामस्वरूप समुद्री धाराएं ऐसे पानी को ध्रुव से दूर ले जाने के लिए तैयार होती हैं। ग्लोबल वार्मिंग का एक संभावित परिणाम यह हो सकता है कि आर्कटिक बर्फ के नष्ट होने के परिणामस्वरूप, इन धाराओं में भी कमी आ सकती है, जिसके कारण निकट और दूर के मौसमों पर अनदेखे असर पड़ सकते हैं।
मिश्रणीयता और संघनन
जल कई तरल पदार्थों जैसे एथेनोल के साथ सभी अनुपातों में विलेयशील होता है और एकमात्र समांगी तरल का निर्माण करता है। दूसरी ओर, जल और अधिकांश तेल अविलेय होते हैं और आम तौर पर शीर्ष से बढ़ते हुए घनत्व के अनुसार परतों का निर्माण करते हैं।
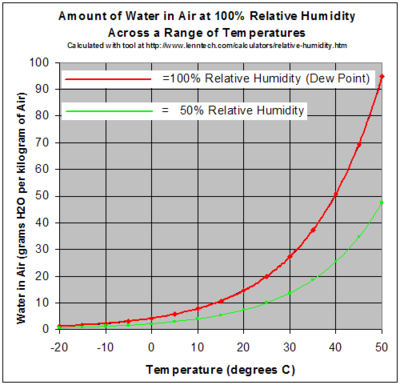
एक गैस के रूप में, जल वाष्प पूरी तरह से वायु में विलेयशील है। दूसरी ओर अधिकतम जल वाष्प दबाव, जो एक निश्चित तापमान पर तरल (या ठोस) के साथ थर्मोडाइनेमिक तरीके से स्थिर रहता है, कुल वायुमंडलीय दबाव की तुलना में अपेक्षाकृत कम रहता है। उदाहरण के लिए, यदि वाष्प का आंशिक दबाव[16] वायुमंडलीय दबाव का 2% है और हवा को 22 °C से शुरू करते हुए 25 °C से ठंडा किया जाता है, तो जल घना होना शुरू हो जाएगा और इससे ओस बिंदु का पता चलेगा और कोहरे या ओस का निर्माण होगा। इसकी प्रतिकूल प्रक्रिया सुबह के समय कोहरे को समाप्त कर देती है। यदि घरेलू तापमान पर नमी को बढ़ाया जाता है तो, मान लीजिये एक गर्म शावर को चलाकर या स्नान से और तापमान एक ही रहता है, तो वाष्प जल्द ही प्रावस्था के परिवर्तन के लिए दबाव में पहुंचता है और भाप के रूप में बाहर आता है। इस सन्दर्भ में एक गैस को संतृप्त या 100% सापेक्षिक आर्द्रता कहते हैं, जब वायु में पानी के भाप का दबाव, अगर (तरल) पानी या पानी (या बर्फ, यदि पर्याप्त ठंडा है) के भाप के दबाव के बराबर है तो वह संतृप्त हवा के संपर्क में आकर वाष्पीकरण के माध्यम से अपनी राशि कम करेगा। चूंकि हवा में भाप की मात्रा कम होती है, सापेक्षिक आर्द्रता, भाप के कारण आंशिक दबाव और संतृप्त जल वाष्प के आंशिक दबाव के बीच का अनुपात काफी उपयोगी हो जाता है। 100% सापेक्षिक आर्द्रता के ऊपर के वाष्प के दबाव को अति-संतृप्त कहा जाता है और यह तब होता है जब हवा तेज़ी से ठंडी होती है, जैसे कभी अचानक ऊपर की तरफ बहाव के साथ.[17]
वाष्प दबाव
दबाव क्षमता
जल की दबाव क्षमता, दबाव और तापमान की एक क्रिया है। 0 °C पर, शून्य दबाव की सीमा में दबाव क्षमता 5.1×१०−10 Pa−1 होती है।[19] शून्य दबाव की सीमा में, दबाव क्षमता, 45 डिग्री सेल्सियस के आसपास एक न्यूनतम 4.4×१०−10 Pa−1 तक पहुंच जाती है, जो बढ़ते तापमान के साथ फिर बढ़ती है। दबाव के बढ़ने के साथ दबाव क्षमता में कमी होती है, 0 डिग्री सेल्सियस और 100 MPa में 3.9×१०−10 Pa−1. जल का थोक मापांक 2.2 GPa है।[20] गैर-गैसों की कम दबाव क्षमता और विशेष रूप से जल, को अक्सर अपरिमेय के रूप में ग्रहण किया जाता है। जल के न्यून दबाव क्षमता का मतलब है कि 4 कि॰मी॰ गहरे समुद्र में, जहां दबाव 40 MPA है, वहां मात्रा में सिर्फ 1.8% की कमी है।[20]
त्रिगुण बिंदु
वह तापमान और दबाव जिस पर तरल, ठोस और गैसीय जल साथ-साथ रहते हैं त्रिगुण बिंदु कहा जाता है। इस बिंदु को तापमान की इकाई परिभाषित करने के लिए इस्तेमाल किया जाता है (केल्विन, थर्मोडाइनेमिक तापमान की SI इकाई, परोक्ष रूप से डिग्री सेल्सियस और डिग्री फेरनहाइट भी)
एक परिणाम के रूप में, जल का त्रिगुण बिंदु तापमान, एक मापी गई मात्रा के बजाय एक निर्धारित मूल्य है।
त्रिगुण बिंदु का तापमान सर्वसम्मति से 273.16 K (0.01 °C) पर है और दबाव 611.73 Pa है। यह दबाव काफी कम है, सामान्य समुद्र स्तर के बैरोमीटर दबाव 101,325 Pa के करीब 1⁄166. मंगल ग्रह पर वायुमंडलीय सतह का दबाव, उल्लेखनीय रूप से त्रिगुण बिंदु दबाव के नज़दीक होता है और मंगल की शून्य-ऊंचाई या "समुद्र स्तर" को उस द्वारा परिभाषित किया जाता है जिस पर वायुमंडलीय दबाव जल के त्रिगुण बिंदु के साथ संगत करता है।
हालांकि इसे सामान्यतः "जल का त्रिगुण बिंदु" कहा जाता है, तरल जल, बर्फ I और जल वाष्प का स्थिर मिश्रण, जल के चरण आरेख पर कई त्रिगुण बिन्दुओं में से एक है। गौटिंगेन में गुस्ताव हेनरिक जोहान अपोलोन तम्मन ने कई अन्य त्रिगुण बिंदुओं पर 20वीं सदी के पूर्वार्ध में डेटा का उत्पादन किया। कम्ब और दूसरों ने 1960 के दशक में त्रिगुण बिन्दुओं को आगे प्रलेखित किया।[21][22][23]
बिजली के गुण
विद्युत चालकता
बिना आयन का शुद्ध जल, एक उत्कृष्ट विसंवाहक है, लेकिन "डीआयनीकृत" जल भी पूरी तरह से आयन मुक्त नहीं है। तरल अवस्था में जल का स्व-आयनीकरण होता है। इसके अलावा, चूंकि जल इतना अच्छा विलायक है कि इसमें लगभग हमेशा कुछ घुला हुआ पदार्थ मिला होता है, अक्सर यह नमक होता है। अगर जल में अशुद्धता की ऐसी थोड़ी भी मात्रा है, तो यह बिजली का अच्छा संचालन करेगा, क्योंकि नमक जैसी अशुद्धियां एक जलकृत घोल में, मुक्त आयन में अलग हो जाती हैं, जिसमें से फिर विद्युत् का प्रवाह हो सकता है।
ये ज्ञात है कि, जल के लिए अधिकतम विद्युत प्रतिरोधकता 25 °C पर लगभग 182 kΩ·m है। यह आंकड़ा, रिवर्स ओसमोसिस पर पाए जाने वाले से काफी मिलता-जुलता है, जहां अल्ट्रा फ़िल्टर्ड और डीआयनीकृत अल्ट्रा शुद्ध जल का प्रयोग किया जाता है, उदाहरण के लिए, अर्धचालक विनिर्माण कारखाने में. एक नमक या एसिड प्रदूषक, जिसका अत्यंत शुद्ध जल में स्तर 100 पार्ट्स पर ट्रीलियन (ppt) है, वह अपनी प्रतिरोधकता स्तर को कई किलोम-मीटर तक कम करना शुरू कर देता है (या प्रति मीटर सैकड़ों नैनोसीमेंस).
जल की निम्न विद्युत् चालकता, आयन-सदृश चीज़ की एक छोटी सी मात्रा से काफी बढ़ जाती है, जैसे हाइड्रोजन क्लोराइड या कोई नमक. इस प्रकार अशुद्धियों वाले जल में इलेक्ट्रोक्युशन का जोखिम अधिक रहता है। यह ध्यान देने लायक है, कि इलेक्ट्रोक्युशन का जोखिम तब कम हो जाता है जब अशुद्धियों का स्तर उस बिंदु तक पहुंच जाता है जब जल, मानव शरीर की अपेक्षा अधिक बेहतर चालक बन जाता है।[कृपया उद्धरण जोड़ें] उदाहरण के लिए, समुद्री जल में इलेक्ट्रोक्युशन का जोखिम, ताजा जल की तुलना में कम हो सकता है, क्योंकि समुद्र में अशुद्धताओं का स्तर बहुत उच्च होता है, विशेष रूप से सामान्य नमक. मुख्य विद्युत् पथ, बेहतर चालक की तलाश करेगा।
जल कि कोई भी विद्युत चालकता, जल में घुले खनिज लवण के आयन और कार्बन डाइऑक्साइड का परिणाम है। कार्बन डाइऑक्साइड, जल में कार्बोनेट आयनों का निर्माण करता है। जल, स्व-आयनीकृत होता है जिसमें जल के दो अणु, एक हाइड्रोकसाइड आयन और एक हाइड्रोनिअम केशन का निर्माण करते हैं, लेकिन इतना पर्याप्त भी नहीं कि जो अधिकांश संक्रियाओं कोई काम या हानि करने लायक विद्युत् धारा का संचालन कर सके। शुद्ध जल में, संवेदनशील उपकरण, 25 °C पर 0.055 µS/cm के मामूली विद्युत चालकता का पता लगा सकता है। जल को ऑक्सीजन और हाइड्रोजन गैसों में इलेक्ट्रोलाइज़ किया जा सकता है, लेकिन घुले हुए आयनों की अनुपस्थिति में यह प्रक्रिया बहुत ही धीमी हो जाती है, क्योंकि बहुत कम धारा का चालन होता है। जबकि जल (और धातुओं) में इलेक्ट्रॉन, चार्ज के प्राथमिक वाहक हैं, बर्फ में प्राथमिक वाहक प्रोटॉन हैं (देखें प्रोटॉन कंडक्टर).
विद्युत अपघटन
जल में एक विद्युत प्रवाह को प्रवाहित करने के माध्यम से, जल को उसके घटक तत्वों, हाइड्रोजन और ऑक्सीजन में विभाजित किया जा सकता है। इस प्रक्रिया को विद्युत अपघटन कहा जाता है। जल के अणु स्वाभाविक रूप से, H+ और OH- आयनों में अलग हो जाते हैं, जो क्रमशः, कैथोड और एनोड की ओर आकर्षित होते हैं। कैथोड पर, दो H+ आयन, इलेक्ट्रॉनों को लेते हैं और H2 गैस का निर्माण करते हैं। एनोड पर, चार OH- आयन संयुक्त होते हैं और O2 गैस, आणविक जल और चार इलेक्ट्रॉनों को छोड़ते हैं। गैसें सतह पर बुलबुले बनती है जहां पर इसे एकत्र किया जा सकता है। जल विद्युत अपघटन सेल की मानक क्षमता 25 डिग्री सेल्सियस पर 1.23 V है।
दोध्रुवीय गुण
जल का एक महत्वपूर्ण गुण उसकी ध्रुवीय प्रकृति है। जल के अणु, एक कोण बनाते हैं जिसमें उनके कोनों पर हाइड्रोजन परमाणु होते हैं और शीर्ष पर ऑक्सीजन. चूंकि, हाइड्रोजन की तुलना में ऑक्सीजन में उच्च वैद्युतीयऋणात्मकता होती है, ऑक्सीजन परमाणु के अणु के सेरों में आंशिक नकारात्मक चार्ज होता है। ऐसी चार्ज भिन्नता वाली किसी वस्तु को डाइपोल कहते हैं। चार्ज भेद, जल के अणुओं को एक दूसरे के प्रति आकर्षित होने को प्रेरित करते हैं (अपेक्षाकृत सकारात्मक क्षेत्र, अपेक्षाकृत नकारात्मक क्षेत्रों को आकर्षित करते हैं) और अन्य ध्रुवीय अणुओं को भी. यह आकर्षण हाइड्रोजन बॉन्डिंग में योगदान देता है और जल के कई गुणों की व्याख्या करता है, जैसे विलायक के रूप में. जल की दो-ध्रुवीय प्रकृति को एक विद्युत प्रवाह युक्त वस्तु को पकड़कर प्रदर्शित किया जा सकता है (जैसे कंघी करने के बाद एक कंघी द्वारा) एक छोटी जल-धारा के पास (उदाहरण के लिए, एक नल से), जिससे पानी की धारा, चार्ज वस्तु की ओर आकर्षित होती है।
हाइड्रोजन बॉन्डिंग
जल का एक अणु अधिकतम चार हाइड्रोजन बांड बना सकता है क्योंकि यह दो हाइड्रोजन परमाणुओं को दे सकता है और ले सकता है। हाइड्रोजन फ्लोराइड, मेथानोल और अमोनिया जैसे अन्य अणु भी हाइड्रोजन बांड बनाते हैं लेकिन वे थर्मोडाइनेमिक, गत्यात्मक या संरचनात्मक गुणों के विषम व्यवहार को प्रदर्शित नहीं करते जैसा कि जल में देखा जाता है। जल और हाइड्रोजन बॉन्डिंग करने वाले अन्य तरल पदार्थ के बीच का स्पष्ट अंतर, इस तथ्य में निहित है कि जल के अलावा अन्य कोई हाइड्रोजन बॉन्डिंग अणु, चार हाइड्रोजन बांड नहीं बना सकता और इसका कारण या तो हाइड्रोजन देने/स्वीकार करने में असमर्थता हो सकती है या फिर बड़ी मात्रा में अवशिष्ट में स्टेरिक प्रभाव हो सकता है। जल में चार हाइड्रोजन बांड के कारण उत्पन्न स्थानीय टेट्राहेड्रल क्रम एक खुली संरचना और एक 3 आयामी बॉन्डिंग नेटवर्क को जन्म देता है, जो 4 °C से नीचे ठंडा किये जाने पर घनत्व में विषम कमी को फलित करता है।
हालांकि, जल के अणु के भीतर कोवैलेंट बांड की तुलना में हाइड्रोजन बॉन्डिंग एक अपेक्षाकृत कमजोर आकर्षण है, यह जल के कई भौतिक गुणों के लिए जिम्मेदार है। एक ऐसा ही गुण है जल का अपेक्षाकृत उच्च गलनांक और क्वथनांक; अणुओं के बीच हाइड्रोजन बांड को तोड़ने के लिए अधिक ऊर्जा की आवश्यकता होती है। इसी तरह मिश्रित हाइड्रोजन सल्फाइड (H2S), जिसमें बहुत कमजोर हाइड्रोजन बॉन्डिंग है, वह एक घरेलू तापमान गैस है, हालांकि इसमें जल की आणविक राशि का दोगुना होता है। जल के अणुओं के बीच अतिरिक्त बॉन्डिंग, तरल जल को एक बड़ी विशिष्ट ताप क्षमता देती है। यह उच्च ताप क्षमता, जल को ताप भंडारण का एक अच्छा मध्यम (शीतलक) और ताप ढाल बनाती है।
पारदर्शिता
दृश्यमान रोशनी, करीब के पराबैंगनी प्रकाश और दूर की लाल रोशनी से अपेक्षाकृत पारदर्शी है, लेकिन यह अधिकांश पराबैंगनी प्रकाश, अवरक्त प्रकाश और माइक्रोवेव को अवशोषित कर लेता है। अधिकांश फोटोरिसेप्टर और फोटोसिंथेटिक रंगद्रव्य, प्रकाश स्पेक्ट्रम के उस हिस्से का उपयोग करते हैं जो जल के माध्यम से अच्छी तरह से संचारित होता है। माइक्रोवेव ओवन जल की अस्पष्टता का लाभ, माइक्रोवेव विकिरण से खाद्य पदार्थों के अंदर के जल को गर्म करने के लिए करते हैं। दृश्यमान स्पेक्ट्रम के अंत के लाल के क्षीण अवशोषण के कारण जल का रंग आतंरिक रूप से नीला दिखता है (जल का रंग देखें).
जुड़ाव
जल आपस में चिपका (जुड़ाव) रहता है क्योंकि यह ध्रुवीय है। अपनी ध्रुवीय प्रकृति के कारण जल में उच्च आसंजन गुण होता है। बेहद साफ/चिकने कांच पर जल, एक पतली परत बना सकता है क्योंकि जल और कांच के अणुओं के बीच (आसंजी बल) ससंजक बल की तुलना में आणविक बल अधिक मजबूत होता है। जैविक कोशिकाओं और ओर्गनेल में, जल का संपर्क झिल्ली और प्रोटीन सतहों से होता है जो हाइड्रोफिलिक होते हैं; यानी कि, वे सतहें जिनका जल के साथ एक मजबूत आकर्षण है। इरविंग लेंगमुइर ने हाइड्रोफिलिक सतहों के बीच एक शक्तिशाली प्रतिकारक बल पाया। हाइड्रोफिलिक सतहों को डीहाईड्रेट करने के लिए - जल के हाईड्रेशन के बलों, बुलाया ताकतों के खिलाफ काम करने की आवश्यकता है, जिसे डीहाईड्रेशन कहते हैं। ये बल बहुत बड़े हैं, लेकिन एक नैनोमीटर या कम के अन्दर तेज़ी से कम हो जाते हैं। वे जीव विज्ञान में महत्वपूर्ण हैं, खासकर जब कोशिकाओं को सूखे वातावरण या फिर निर्जलित करके सुखाया जाता है।[24]
सतही तनाव
जल में घरेलू तापमान पर 72.8 mN/m का एक उच्च सतही तनाव होता है, जो जल के अणुओं के बीच मजबूत संशक्ति के कारण होता है और गैर-धातु तरल पदार्थों में यह उच्चतम है। देखा जा सकता है जब पानी की थोड़ी सी मात्रा को शोषण मुक्त (गैर-अधिषोशी और गैर-अवशोषी) सतह पर डाला जाए, जैसे कि पोलीथिलीन या टेफ्लॉन और जल, बूंद के रूप में एक साथ बना रहता है। महत्वपूर्ण रूप से जल की सतह में फंसी हुई हवा, बुलबुले बना देती है, जो कभी-कभी लंबे समय तक रह कर गैस अणुओं को हस्तांतरित करता है।[कृपया उद्धरण जोड़ें]
एक और सतही तनाव केशिका लहर है, जो सतह पर जल की बूंदों के असर के आसपास बनाते हैं और कभी-कभी मजबूत धाराओं के रूप में सतह पर बहते हैं। पृष्ठ तनाव के कारण उत्पन्न प्रत्यास्थता, केशिका लहर को जन्म देती है।
कैपिलरी क्रिया
आसंजन और सतही तनाव के परस्पर बलों के कारण, जल केशिका क्रिया प्रदर्शित करता है जिसके तहत गुरुत्वाकर्षण बल के खिलाफ, जल एक संकीर्ण ट्यूब में ऊपर उठता है। जल, ट्यूब की अंदरी दीवार से लगा रहता है और सतही तनाव सतह को सीधा रखते हुए उसे ऊपर उठाता है और संशक्ति के माध्यम से और अधिक जल ऊपर खींच लिया जाता है। यह प्रक्रिया जारी रहती है जब तक कि जल ट्यूब में बहता रहता है और फिर बाद में गुरुत्वाकर्षण बल आसंजक बालों को संतुलित करता है।
सतही तनाव और केशिका क्रिया, जीव विज्ञान में महत्वपूर्ण हैं। उदाहरण के लिए, जब जाइलम के माध्यम से जल को पौधों में ऊपर ले जाया जाता है, तो मजबूत अंतर-आणविक आकर्षण (ससंजन) जल के भागों को एक साथ पकड़े रहता है और आसंजन गुण, जाइलम से जल का सम्बन्ध बनाए रखता है और स्वेद खिंचाव द्वारा होने वाले तनाव टूटन को रोकता है।
एक विलायक के रूप में जल
अपनी ध्रुवीयता के कारण जल एक अच्छा विलायक भी है। जो पदार्थ जल में अच्छी तरह मिल जाते हैं और घुल जाते हैं (जैसे नमक) उन्हें हाइड्रोफिलिक ("जल-प्रेमी") के रूप में जाना जाता है और जो नहीं घुलते हैं (जैसे वसा और तेल) उन्हें हाइड्रोफोबिक ("जल भयभीत") के रूप में जाना जाता है। किसी पदार्थ के जल में घुलने की क्षमता का निर्धारण इस बात से होता है क्या वह पदार्थ जल द्वारा जनित अणुओं से मिलता है या उनसे बेहतर है। यदि किसी पदार्थ के गुण मज़बूत अंतर-आणविक बलों पर काबू पाने की अनुमति नहीं देते हैं, अणुओं को जल से "बाहर धक्का दे दिया" जाता है और वे घुलते नहीं हैं। आम धारणा के विपरीत, जल और हाइड्रोफोबिक पदार्थ, "विकर्षण" नहीं उत्पन्न करते हैं और एक हाइड्रोफोबिक सतह का हाईड्रेशन, शक्तिशाली रूप से अनुकूल होता है।
जब एक आयनिक या ध्रुवीय यौगिक, जल में प्रवेश करता है, तो यह जल के अणुओं (हाईड्रेशन) द्वारा घिरा होता है। जल के अपेक्षाकृत छोटे आकार के अणु, आम तौर पर जल के कई अणुओं को विलेय के एक अणु के चारों ओर इकठ्ठा होने की अनुमति देते हैं। जल के, आंशिक रूप से नकारात्मक डाइपोल छोर, विलेय के सकारात्मक चार्ज वाले घटकों की ओर आकर्षित होते हैं और इसका ठीक उलटा सकारात्मक डाइपोल के छोरों पर लागू होता है।
सामान्यतः, आयनिक और ध्रुवीय पदार्थ जैसे, एसिड, शराब और नमक, जल में अपेक्षाकृत घुलनशील हैं और गैर-ध्रुवीय पदार्थ जैसे वसा और तेल नहीं हैं। गैर ध्रुवीय अणु, जल में एक साथ इसलिए रहते हैं क्योंकि जल के अणुओं के लिए यह अधिक अनुकूल है कि वे एक दूसरे से हाइड्रोजन बूंद करें, बजाय इसके कि गैर-ध्रुवीय अणुओं के साथ वे वैन डेर वॉल संपर्क में संलग्न हों.
आयनिक विलेय का एक उदाहरण है टेबल नमक; सोडियम क्लोराइड, NaCl, जो Na+ कैशन और Cl- आयनों में अलग हो जाता है, जिसमें से प्रत्येक जल के अणु से घिरा रहता है। आयनों को फिर आसानी से उनके स्फटिक लैटिस से दूर ले जाया जाता है। सामान्य चीनी एक गैर-आयनिक विलेय का उदाहरण है। जल के डाईपोल, चीनी के अणु (OH समूह) के ध्रुवीय क्षेत्रों के साथ हाइड्रोजन बांड बनाते हैं और इसे घोल में जाने की अनुमति देते हैं।
एसिड-आधारित अभिक्रिया में जल
रासायनिक रूप से, जल उभयधर्मी है: यह रासायनिक अभिक्रियाओं में या तो एक बेस या एक अम्ल का कार्य कर सकता है। ब्रोंस्तेद-लोरी परिभाषा के अनुसार, एक एसिड को एक ऐसी प्रजाति के रूप में परिभाषित किया गया है जो एक अभिक्रिया में एक प्रोटॉन का दान करता है (एक H+ आयन) और एक बेस का जो प्रोटॉन लेता है। जब एक मजबूत एसिड के साथ अभिक्रिया होती है तो जल एक बेस के रूप में कार्य करता है; जब एक मजबूत बेस के साथ अभिक्रिया होती है तो यह एक एसिड के रूप में कार्य करता है। उदाहरण के लिए, जब हाइड्रोक्लोरिक एसिड बनता है तो जल एक H+ आयन HCL से प्राप्त करता है:
- HCL (एसिड) + H2O (बेस)
 H3O+ + Cl-
H3O+ + Cl-
अमोनिया के साथ प्रतिक्रिया में, NH3, जल एक H+ आयन देता है और इस प्रकार एक एसिड के रूप में कार्य करता है:
- NH3 (आधार) + H2O (एसिड)
 NH4+ + OH-
NH4+ + OH-
चूंकि जल के ऑक्सीजन परमाणु में दो अकेली जोड़ी होती है, जल अक्सर, एक लुईस एसिड के साथ प्रतिक्रियाओं में एक लुईस बेस या इलेक्ट्रॉन जोड़ी दाता के रूप में कार्य करता है, हालांकि यह लुईस बेस के साथ भी प्रतिक्रिया कर सकता है और इलेक्ट्रॉन जोड़ी दाता और जल के हाइड्रोजन परमाणुओं के बीच हाइड्रोजन बांड बना सकता है। HSAB सिद्धांत, जल को एक कमजोर कठोर एसिड और एक कमजोर कठोर बेस के रूप में वर्णित करता है, जिसका अर्थ है कि यह अन्य कठोर प्रजाति के साथ इच्छानुसार प्रतिक्रिया करता है:
- H+ (लुईस एसिड) + H2O (लुईस बेस) → H3O+
- Fe3+ (लुईस एसिड) + H2O (लुईस बेस) → Fe(H2O)63+
- Cl- (लुईस बेस) + H2O (लुईस एसिड) → Cl(H2O)6-
जब एक कमजोर बेस या एक कमजोर एसिड का नमक जल में घुलता है, तो जल आंशिक रूप से नमक को हाइड्रोलाइज कर सकता है, जो साबुन के जलकृत मिश्रण और बेकिंग सोडा को उनका मूल pH देता है:
- Na2CO3 + H2O
 NaOH + NaHCO3
NaOH + NaHCO3
लिगेंड रसायन
जल का लुईस आधार, इसे संक्रमण में एक आम लिगेंड बनाता है, जिसके उदाहरण हैं विलायक आयन, जैसे Fe(H2O)63+, साथ ही पेर्हेनिक एसिड और विभिन्न ठोस हाइड्रेट्स, जैसे CoCl2·6H2O. जल, आम तौर पर एक मोनोडेंट लिगेंड है, यह केंद्रीय एटम के साथ केवल एक ही बौंड बनाता है।
कार्बनिक रसायन
कठोर आधार के रूप में जल, के कार्बनिक कार्बोकेशन के साथ तत्काल प्रतिक्रिया करता है, उदाहरण के लिए, हाईड्रेशन अभिक्रिया में, जिसमें हाइड्रॉक्सिल समूह (OH-) और एक अम्लीय प्रोटॉन को कार्बन-कार्बन डबल बांड में एक साथ बंधे दो कार्बन परमाणुओं में जोड़ा जाता है जिसके परिणामस्वरूप शराब प्राप्त होती है। जब कार्बनिक अणु में जल का मिश्रण, अणु को दो में विभाजित करता है तो इसे हाइड्रॉलिसिस कहा जाता है। हाइड्रोलिसिस के उल्लेखनीय उदाहरण में शामिल है पोलीसैकराइड और प्रोटीन का पाचन और साबुन निर्माण में वसा प्रयोग. जल, SN2 प्रतिस्थापन और E2 उन्मूलन प्रतिक्रियाओं में लीविंग ग्रुप हो सकता है, बाद वाले को निर्जलीकरण प्रतिक्रिया के रूप में जाना जाता है।
प्रकृति में अम्लता
शुद्ध जल में हाइड्राक्साइड आयनों (OH-) का संकेंद्रण है जो हाइड्रोनियम के बराबर है (H3O+) या हाइड्रोजन (H+) आयनों के, जो 298 K में 7 का pH देता है। व्यवहार में, शुद्ध जल का निर्माण करना बहुत मुश्किल है। हवा के संपर्क में छोड़े गए जल में कार्बन डाइऑक्साइड घुल जाता है, जो कार्बोनिक एसिड का मिश्रण बनाता है जिसका सीमित pH करीब 5.7 होता है। जब वातावरण में बादल की बूंदे बनती हैं और जब वर्षा की बूंदे हवा के माध्यम से होते हुए नीचे गिरती हैं तो CO2 की मामूली मात्रा अवशोषित हो जाती है और इस प्रकार अधिकांश बारिश थोड़ा अम्लीय होती है। यदि हवा में नाइट्रोजन और सल्फर आक्साइड की मात्रा अधिक है तो वे भी बादलों में घुल जायेंगे और अम्लीय वर्षा का निर्माण होगा।
रेडोक्स अभिक्रियाओं में जल
जल में ऑक्सीकरण अवस्था +1 में हाइड्रोजन और ऑक्सीकरण अवस्था -2 में ऑक्सीजन होता है। इस कारण से, जल रसायनों को H+/H2 की क्षमता से नीचे घटाव क्षमता के साथ ओक्सीडाइज करता है, जैसे की हाईड्राईड, एल्कली और
अल्कलाइन धातु (बेरिलिअम को छोड़कर). कुछ अन्य प्रतिक्रियाशील धातु, जैसे एल्यूमीनियम, को जल से ओक्सीडाइज किया जाता है, लेकिन उनका आक्साइड, घुलनशील नहीं है और प्रतिक्रिया, पेसिवेशन की वजह से रुक जाती है। ध्यान दें, लोहे में जंग लगना लोहे और ऑक्सीजन के बीच एक प्रतिक्रिया है, पानी में घुल कर, न कि लोहे और जल के बीच.
- 2 Na + 2 H2O → 2 NaOH + H2
ऑक्सीजन गैस का उत्सर्जन करते हुए, जल खुद ही ओक्सिडाइज हो सकता है, लेकिन बहुत कम ही ओक्सीडेंट जल के साथ प्रतिक्रिया करते हैं, भले ही उनकी घटाव क्षमता O2/O2- से अधिक हो। लगभग सभी ऐसी प्रतिक्रियाओं को एक उत्प्रेरक की आवश्यकता होती है।[26]
- 4 AgF2 + 2 H2O → 4 AgF + 4 HF + O2
भू-रसायनशास्त्र
चट्टान पर जल की लंबी अवधि तक चलने वाली क्रिया के कारण आम तौर पर अपक्षय और जल कटाव होता है, ये प्रक्रियाएं ठोस चट्टानों और खनिजों को मृदा और तलछट में परिवर्तित कर देती हैं, लेकिन कुछ स्थितियों में जल के साथ रासायनिक अभिक्रियाएं भी होती हैं, जिसके परिणामस्वरूप मेटासोमेटिज्म या खनिज हाईड्रेशन होता है, यह पत्थर का एक रासायनिक परिवर्तन है जो और प्रकृति में मृदा खनिज पैदा करता है और तब भी होता है जब पोर्टलैंड सीमेंट कठोर हो जाता है।
जलीय बर्फ, क्लाथ्रेट यौगिकों का निर्माण कर सकते हैं जिन्हें क्लाथ्रेट हाइड्रेट्स कहा जाता है, जिसमें छोटे अणुओं की किस्में होती हैं जिन्हें उसके क्रिस्टल लैटिस में जड़ा जा सकता है। इनमें सबसे उल्लेखनीय है मीथेन क्लाथ्रेट, 4 CH4·23H2O, स्वाभाविक रूप से सागर ताल में बड़ी मात्रा में पाया जाता है।
भारी जल और आइसोटोपोलोग्स
ऑक्सीजन और हाइड्रोजन, दोनों के कई आइसोटोप मौजूद हैं, जो जल के कई ज्ञात आइसोटोपोलोग्स को बढ़ा रहे हैं।
हाइड्रोजन, स्वाभाविक रूप से तीन समस्थानिक में होता है। सबसे आम (¹H), जो जल में हाइड्रोजन की 99.98% से अधिक मात्रा के लिए जिम्मेदार है, अपने नाभिक में केवल एक प्रोटॉन से बना हैं। एक दूसरा, स्थिर आइसोटोप, ड्यूटेरिअम (रासायनिक चिह्न D या ²H), में एक अतिरिक्त न्यूट्रॉन होता है। ड्यूटेरिअम ऑक्साइड,D2O, को इसके उच्च घनत्व की इसकी वजह से इसे भारी जल के रूप में भी जाना जाता है। इसे परमाणु रिएक्टर में न्यूट्रॉन मंदक के रूप में प्रयोग किया जाता है। तीसरे आइसोटोप, ट्रिटियम में 1 प्रोटॉन और 2 न्यूट्रॉन हैं और यह रेडियोधर्मी है, जो 4500 दिन के अर्ध-जीवन में खराब हो जाता है। T2O प्रकृति में बहुत थोड़ी मात्रा में मौजूद है, जो मुख्यतः कॉस्मिक किरण जनित परमाणु अभिक्रिया द्वारा वातावरण में उत्पन्न होते हैं। जल, जिसमें एक ड्यूटेरिअम परमाणु HDO होता है, साधारण जल में स्वाभाविक रूप से न्यून संकेन्द्रण (~0.03%) के साथ होता है और D2O में काफी कम मात्रा में (0.000003%).
विशिष्ट राशि के अंतर के अलावा, H2O और D2O के बीच सबसे उल्लेखनीय भौतिक मतभेद में ऐसे गुण शामिल हैं जो हाइड्रोजन बॉन्डिंग से प्रभावित होते हैं, जैसे हिमीकरण और खौलाना और अन्य गत्यात्मक प्रभाव. क्वथनांक में अंतर आइसोटोपोलोग्स को अलग किये जाने की अनुमति देता है।
शुद्ध पृथक D2O की खपत, जैव रासायनिक प्रक्रियाओं को प्रभावित कर सकती हैं - बड़ी मात्रा में इसका सेवन करने से गुर्दे और केंद्रीय तंत्रिका तंत्र नष्ट हो सकते है। छोटी मात्रा में इसका सेवन, बिना किसी बुरे प्रभाव के किया जा सकता है और किसी भी विषाक्तता के स्पष्ट होने के लिए बड़ी मात्रा में भारी जल का सेवन करना होगा।
ऑक्सीजन के भी तीन स्थिर आइसोटोप हैं, 16O 99.76% में मौजूद है, 17O 0.04% में और 18O जल के 0.2% अणुओं में.[27]
इतिहास
विद्युत्-अपघटन द्वारा जल का हाइड्रोजन और ऑक्सीजन में पहली बार विघटन, अंग्रेजी रसायनज्ञ विलियम निकोल्सन द्वारा 1800 में किया गया था। 1805 में, जोसेफ लुइस गे-लुसाक और अलेक्जेंडर वॉन हम्बोल्ट ने दिखाया कि कि जल का निर्माण हाइड्रोजन के दो भागों और ऑक्सीजन के एक भाग से बना है।
गिल्बर्ट न्यूटन लुईस ने 1933 में शुद्ध भारी जल का पहला नमूना अलग किया।
जल के गुणों का इस्तेमाल ऐतिहासिक रूप से विभिन्न तापमान स्केलों को परिभाषित करने के लिए किया जाता रहा है। विशेष रूप से, केल्विन, सेल्सियस, रैंकिन और फारेनहाइट स्केल को अतीत या वर्तमान में जल के हिमांक और क्वथनांक से परिभाषित किया जाता है। अपेक्षाकृत कम लोकप्रिय थर्मामीटर और डेलिस्ले, न्यूटन, रौयमर और रोमेर को इसी प्रकार परिभाषित किया गया। जल का त्रिगुण बिंदु आज एक अधिक सामान्यतः प्रयोग किया जाने वाला मानक बिंदु है।[28]
व्यवस्थित नामकरण
स्वीकार किया गया जल का IUPAC नाम ओक्सिडेन है[29] या बस जल, या अलग-अलग भाषाओं में इसका समकक्ष, हालांकि कई अन्य व्यवस्थित नाम हैं जिनका प्रयोग अणुओं का वर्णन करने के लिए किया जा सकता है।[30]
जल का सबसे अच्छा व्यवस्थित नाम हाइड्रोजन ऑक्साइड है। यह हाइड्रोजन सल्फाइड, हाइड्रोजन पेरोक्साइड और ड्यूटेरीअम ऑक्साइड (भारी जल) जैसे संबंधित यौगिकों के अनुरूप है। एक और व्यवस्थित नाम ओक्सिडेन को IUPAC द्वारा ऑक्सीजन आधारित प्रतिस्थापक समूह के व्यवस्थित नामकरण के जनक नाम के रूप में स्वीकार किया गया है,[31] हालांकि आमतौर पर इनके भी अन्य सिफारिश नाम हैं। उदाहरण के लिए, -OH समूह के लिए, हाइड्रोक्सिल नाम को ओक्सीडेनिल की तुलना में अधिक तरजीह दी जाती है। ओक्सेन नाम को, इस उद्देश्य के लिए IUPAC द्वारा स्पष्ट रूप से अनुपयुक्त करार दिया गया है, क्योंकि यह पहले से ही टेट्राहाइड्रोपाईरेन नाम के चक्रीय ईथर का नाम है।
जल के अणु का ध्रुवीय रूप, H+OH-, को IUPAC नामकरण के अनुसार हाईड्रोन हाइड्रोक्साइड भी कहा जाता है।[32]
डीहाइड्रोजन मोनोऑक्साइड (DHMO) जल का एक पंडिताऊ नामकरण है। यह शब्द रासायनिक अनुसंधान की पेरोडीज़ में प्रयोग किया गया है जिसमें इस "घातक रसायन" के इस्तेमाल पर रोक लगाने की मांग की गई है, जैसे कि डीहाइड्रोजन मोनोऑक्साइड होक्स में. जल के अन्य व्यवस्थित नाम में शामिल हैं हाईड्रोक्सिक एसिड, हाईड्रोक्सिलिक एसिड, और हाइड्रोजन हाइड्रोक्साइड . जल के लिए, एसिड और क्षार, दोनों नाम मौजूद हैं, क्योंकि यह उभयधर्मी है (क्षार या एसिड, दोनों रूपों में अभिक्रिया करने में सक्षम है). हालांकि ये नाम तकनीकी रूप से गलत नहीं हैं, उनमें से कोई भी व्यापक रूप से इस्तेमाल नहीं होता है।
जल के कुछ सामग्री सुरक्षा डेटा पत्रक, जल में डूबने को एक खतरे के रूप में सूचीबद्ध करते हैं।[33][34]
इन्हें भी देखें
सन्दर्भ
- ↑ अ आ Braun, Charles L.; Sergei N. Smirnov (1993). "Why is water blue?". J. Chem. Educ. 70 (8): 612. मूल से 3 अप्रैल 2012 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ अ आ Vienna Standard Mean Ocean Water (VSMOW), used for calibration, melts at 273.1500089(10) K (0.000089(10) °C, and boils at 373.1339 K (99.9839 °C)
- ↑ "संयुक्त राष्ट्र". मूल से 14 मई 2011 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ रे: वाट परसेंटेज ऑफ़ दी युमन बोडी इज कंपोज्ड ऑफ़ वाटर ? जेफ्री उत्ज़, एमडी, मेडसाईं नेटवर्क
- ↑ Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006). Biology: Exploring Life. Boston, Massachusetts: Pearson Prentice Hall. आई॰ऍस॰बी॰ऍन॰ 0-13-250882-6. मूल से 2 नवंबर 2014 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ Smith, Jared D. (2005). "Unified description of temperature-dependent hydrogen bond rearrangements in liquid water"" (PDF). Proc. Natl. Acad. Sci. 102 (40): 14171–14174. डीओआइ:10.1073/pnas.0506899102. मूल(PDF) से 1 नवंबर 2018 को पुरालेखित. अभिगमन तिथि 12 मई 2010. नामालूम प्राचल
|coathors=की उपेक्षा की गयी (मदद) - ↑ "Heat of Vaporization of Water vs. Temperature". मूलसे 20 दिसंबर 2016 को पुरालेखित. अभिगमन तिथि 14 जून 2020.
- ↑ "Constant pressure heat capacity of water vs. temperature". मूल से 30 अप्रैल 2012 को पुरालेखित. अभिगमन तिथि 14 जून 2020.
- ↑ लिडे, डॉ॰ (एड.) (1990). रसायन विज्ञान और भौतिकी की CRC हैंडबुक (70 Edn).. बोका रटन (FL): CRC प्रेस.
- ↑ "Water - Density and Specific Weight". मूल से 12 मई 2015 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ Shell, Scott M.; Pablo G. Debenedetti, Athanassios Z. Panagiotopoulos (2002). "Molecular structural order and anomalies in liquid silica" (PDF). Phys. Rev. E Stat. Nonlin. Soft. Matter. Phys. 66: 011202. डीओआइ:10.1103/PhysRevE.66.011202. मूल(PDF) से 4 जून 2016 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ "विजयी रसायन विज्ञान, 4 एड., 2004. http://www.cci.net.au/conqchem/ Archived 2012-04-26 at the Wayback Machine
- ↑ पी जी देबेनदेत्ती, स्नातकोत्तर और स्टेनली, महामहिम, "और ग्लासी शीतल जल," भौतिकी आज 56 (6), पी. 40-46 (2003).
- ↑ "IAPWS, Release on the pressure along the melting and the sublimation curves of ordinary water substance, 1993"(PDF). मूल (PDF) से 7 दिसंबर 2004 को पुरालेखित. अभिगमन तिथि 2008-02-22.
- ↑ "Thermal Conductivity of some common Materials". मूल से 25 जुलाई 2017 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ हवा में जल वाष्प के कारण होने वाले दबाव को आंशिक दबाव कहा जाता है (डाल्टन नियम) और यह हवा में जल के अणुओं के संकेन्द्रण के आनुपातिक है (बौयल का नियम).
- ↑ अडियाबेटिक शीतलन कानून गैस जिसके परिणामस्वरूप से आदर्श है।
- ↑ ब्राउन, थिओडोर एल, एच. यूजीन लेमे, जूनियर और ब्रूस ई. बर्स्तान . रसायन विज्ञान: केंद्रीय विज्ञान. एड 10. ऊपरी सैडल नदी, NJ: पिअरसोंन शिक्षा, Inc, 2006.
- ↑ Fine, R.A. and Millero, F.J. (1973). "Compressibility of water as a function of temperature and pressure". Journal of Chemical Physics. 59 (10): 5529. डीओआइ:10.1063/1.1679903.
|pages=और|page=के एक से अधिक मान दिए गए हैं (मदद) - ↑ अ आ Oliver Schlüter (2003-07-28). "Impact of High Pressure — Low Temperature Processes on Cellular Materials Related to Foods" (PDF). Technischen Universität Berlin. Archived 2008-03-09 at the Wayback Machine
- ↑ Gustav Heinrich Johann Apollon Tammann (1925). "The States Of Aggregation". Constable And Company Limited.
- ↑ William Cudmore McCullagh Lewis and James Rice (1922). A System of Physical Chemistry. Longmans, Green and co.
- ↑ "Physical Forces Organizing Biomolecules (PDF)"(PDF). मूल (PDF) से 11 अक्तूबर 2004 को पुरालेखित. अभिगमन तिथि 11 अक्तूबर 2004.
- ↑ Surface Tension of Water vs. Temperature[मृत कड़ियाँ]
- ↑ G. Charlot (2007). Qualitative Inorganic Analysis. Read Books. पृ॰ 275. आई॰ऍस॰बी॰ऍन॰ 1406747890. मूल से 3 जून 2013 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ IAPWS (2001). "Guideline on the Use of Fundamental Physical Constants and Basic Constants of Water" (PDF). मूल (PDF) से 28 जनवरी 2017 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ "A Brief History of Temperature Measurement". मूल से 13 जनवरी 2004 को पुरालेखित. अभिगमन तिथि 13 जनवरी 2004.
- ↑ Mononuclear hydrides Archived 2010-12-12 at the Wayback Machine गाइड में एक ACDLabs संस्करण द्वारा ऑनलाइन करने के लिए IUPAC नामकरण कार्बनिक यौगिकों की 1993) अनुशंसाएँ (
- ↑ "संग्रहीत प्रति". मूल से 23 फ़रवरी 2012 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ ले, जीजे एट अल. 1998 . Principles of chemical nomenclature: a guide to IUPAC recommendations,Archived 2009-09-29 at the Wayback Machine, पी. 99. ब्लैकवेल विज्ञान लिमिटेड, ब्रिटेन. ISBN 0-86542-685-6
- ↑ "hydron hydroxide compound summary at PubChem". मूल से 2 मई 2013 को पुरालेखित. अभिगमन तिथि 12 मई 2010.
- ↑ MSDS David Grays Distilled Water 060106.pdf, स्वास्थ्य - प्रभाव: सांस"... अत्यधिक सांस लेना डूबने का कारण हो सकता है।"
- ↑ MSDS for battery water Archived 2008-02-24 at the Wayback Machine, धारा छठे - स्वास्थ्य खतरा डेटा: "जल डूबने से मौत का कारण हो सकता"
बाहरी कड़ियाँ
- Release on the IAPWS Industrial Formulation 1997 for the Thermodynamic Properties of Water and Steam (तेज अभिकलन गति)
- Release on the IAPWS Formulation 1995 for the Thermodynamic Properties of Ordinary Water Substance for General and Scientific Use (सरल निर्माण)
- Sigma Xi The Scientific Research Society, Year of Water 2008
- Stockholm International Water Institute (SIWI)
- Chaplin, Martin. "Water Structure and Science". London South Bank University. मूल से 3 मई 2010 को पुरालेखित. अभिगमन तिथि 2009-07-07.
- जल के vapor pressure, liquid density, dynamic liquid viscosity, surface tension की गणना











.jpeg)

No comments:
Post a Comment